近日,喜讯连连,由微珂咨询牵头并共同参与的经皮神经电刺激器Transcuataneous electrical nerve stimulation(简称TENS)项目成功获美国食品药品监督管理局(FDA)510k批准。项目从FDA接受资料开始评审到批准,前后62天,一次性通过。

所谓的FDA510K编码是美国食品药品化枚品(FDC)行动委员会的法案章,这个法案的章恰好在美国FDC法案的第510章所以很多人习惯性的叫它510K,而这是美国食品药品化妆品(FDC)行动委员会法案所以大家都喜欢叫它FDA。根据本法案第510K节的要求,所有引入美国市场的规定器械都要符合本法案的要求而那些未被豁免510K的一类、二类或三类医疗器械必须进行产品上市注册,所以这种产品上市注册俗称FDA510K认证。
什么是FDA-510k ?
FDA-510K,是美国食品、药品和化妆品(FD&C)行动委员会的一个法案章节,而这个法案的章节,正好是在美国FD&C Act第510章节,所以很多人习惯性的把他称作是510K,而且这个是美国食品、药品和化妆品(FD&C)行动委员会法案,所以大家又都喜欢叫它做FDA510K,这就是所谓的FDA510K的由来。
因为根据这个510K章节的法案要求,凡是把一些规定的器械引入美国市场,都要求满足这个法案,那些不豁免510k的I类或II类或III类医疗器械,都必须做“产品上市登记”。所以这个产品上市登记,就是通常我们称做的FDA510(K)认证。
谁必须递交 FDA-510(k)
食品、药品和化妆品(FD&C)行动委员会和21 CFR 807的510(k)规章中并没有特别指出谁必须申请510(k)——任何人都可以申请。
但是,他们指定了哪种行为,例如把器械引入美国市场,要求510(k)申请。
基于指定的行为,必须向FDA递交510(k)的如下所示:
1) 把器械引入美国市场的国内厂家;
如果成品器械厂家根据他们自己的规范装配器械,并在美国上市,那么必须递交510(k)。然而,器械组件厂家并不要求递交510(k),除非这些组件销售给终用户作为替换零件。
合同厂家,这些公司根据其他的规范按照合同装配器械,不要求递交510(k)。
2) 把器械引入美国市场的规范制订者;
FDA审查规范制订者与审查厂家几乎一样。规范制订者是制订成品器械规范的人,但是器械按照合同由其他的公司来生产。因此,规范的制订者,而不是合同厂家需要递交510(k)。
3) 改变标注或操作严重影响器械的再包装者或再标注者;
如果再包装者或再标注者严重改变了标注或影响了器械的其他条件,可能会要求递交上市前通知书。此时,你必须确定是否通过修改指南,删除或增加了警告,禁忌征候等等而显著改变了标注,还有包装操作是否能够改变器械的条件。然而,大多数的再包装者或再标注者并不要求递交510(k)。
4) 把器械引入美国市场的外国厂家/出口商或外国厂家/出口商的美国代理方。
何时需要510(k)
在下列情况下需要递交510(k):
第一次进行商业分配(上市)。在1976年5月28日之后(FD&C Act进行医疗器械修正的有效日期),任何想在美国出售医疗器械的人都要求在器械上市之前至少90天递交510(k)申请。如果器械在1976年5月28日之前不是由你的公司上市的,要求递交510(k)。
对于已上市器械提出不同的使用目的。510(k)规范(21 CFR 807)对于使用目的的主要变化,特别要求递交上市前通知书。使用目的在器械的标注或广告的声明中指出。然而,如果使用意图没有全部发生变化,大多数的变化都需要递交510(k)。
已上市器械发生改变或改进,如果这个改变能够严重影响器械的安全性或有效性的情况下。
申请人负责决定改进是否能够严重影响器械的安全性或有效性。无论得出怎样的结论,都要做纪录,此记录能够在器械主记录中反应出来,在医疗器械质量管理规范的要求下,改变控制记录。如果被询问到,申请者就能够证明评估了这个改动。
对现有器械进行了显著影响器械安全性或有效性的改变或改动,或者上市器械的指南为全新的,或与原来不同的情况下,要求递交新的,完整的510(k)文件。
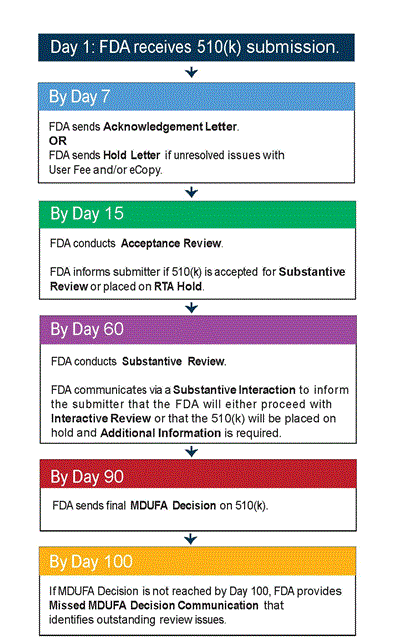
510(k)
微珂将协助您完成510(k)的整个申请,并让您的产品最终获得美国FDA的批准,获得进入美国市场的入场券。